Patrice Courvalin, Unite des Agents Antibacteriens, Institut Pasteur, 25-28 rue du Docteur Roux, г. Париж (Франция)
Пробиотики, используемые для профилактики кишечных расстройств, могут приобрести полирезистентность к антибиотикам, что позволяет им выжить в условиях одновременного приема этих препаратов. Однако при этом возникает вероятность переноса генов резистентности от пробиотика к патогенными для человека микроорганизмам как непосредственно, так и опосредованно через комменсальную микрофлору. В данной статье рассматриваются эксперименты, которые необходимо провести, а также критерии оценки безопасности антибиотикорезистентных пробиотиков.
С целью профилактики побочных явлений со стороны желудочно-кишечного тракта, вызванных пероральной антибиотикотерапией, пациентам достаточно часто назначают бактериальные пробиотики. В настоящее время широко распространено мнение о том, что при приеме внутрь больших количеств микроорганизмов, например Lactobacillus или Bifidobacterium, или бактериальных спор (микроорганизмов вида Bacillus) микрофлора кишечника, нарушенная под действием антибиотиков, может восстановиться [1].
Однако применение пробиотиков может сопровождаться появлением непредвиденных побочных эффектов, таких как развитие интеркуррентного заболевания вследствие воздействия токсинов, вырабатываемых пробиотиками; или, что отмечается гораздо реже, возникновением инфекционного заболевания, вызванного самим микроорганизмом. Одним из отдаленных последствий терапии, которому до недавнего времени уделялось мало внимания, является распространение генов антибиотикорезистентности среди патогенных микроорганизмов. В этой статье мы рассмотрим потенциальные последствия применения полирезистентных пробиотиков в отношении характера бактериальной резистентности микроорганизмов, способных вызывать заболевания у человека.
Существует два типа бактериальной антибиотикорезистентности: истинная (первичная) и приобретенная [2]. Истинная, или природная, резистентность (ее правильнее называть нечувствительностью) имеется у всех штаммов конкретного рода или вида; она ограничивает спектр бактериальной активности конкретного антибиотика. Эта резистентность является хромосомно-опосредованной и не может передаваться другим бактериям.
В отличие от истинной приобретенная резистентность возникает только у незначительной части микроорганизмов, относящихся к конкретному роду или виду. Иногда это количество может быть достаточно высоким, как в случае резистентности Staphylococcus aureus к бензилпенициллину вследствие выработки пенициллиназы. Приобретенная резистентность может возникать в результате действия двух различных механизмов: мутаций в конституциональных генах (генах «домашнего хозяйства» – housekeeping genes; в этом случае передача гена резистентности не происходит); а также приобретения экзогенных детерминант резистентности от других микроорганизмов путем горизонтального (латерального) переноса генов (в этом случае возможна дальнейшая передача гена).
Примером этому может служить резистентность к ванкомицину, характерная для некоторых лактобактерий и Enterococcus faecium. Что касается лактобактерий, то некоторые их виды вырабатывают пептидогликан, ответственный за нечувствительность к ванкомицину; а в случае с E. faecium, который обычно является чувствительным к ванкомицину, резистентность является приобретенной и плазмидоопосредованной [3, 4]. Понятно, что последствия с точки зрения безопасности в этих двух случаях будут разными.
Полирезистентность к антибиотикам и безопасность пробиотиков
Пробиотики могут обладать чувствительностью к большинству антибиотиков (за исключением тех, к которым у них имеется истинная нечувствительность), а могут иметь природную полирезистентность или приобрести ее искусственным путем. Полирезистентные пробиотики могут применяться одновременно с антибиотиками для профилактики возникновения побочных явлений со стороны желудочно-кишечного тракта, вызванных пероральными антибиотиками. Однако такой подход имеет ряд недостатков.
· Существует вероятность переноса генов резистентности от пробиотика к микроорганизмам, патогенным для человека как непосредственно, так и опосредованно через комменсальную микрофлору.
· Сами пробиотики могут приобретать гены резистентности от бактерий-комменсалов, живущих в организме человека.
· В случае возникновения инфекций, вызванных самим пробиотиком (наблюдается очень редко и преимущественно у лиц с иммунодефицитом), наличие полирезистентного штамма может существенно сократить спектр антибиотиков, пригодных для лечения такого пациента.
Следует особо подчеркнуть, что живые микроорганизмы, используемые в качестве пищевых добавок, по меньшей мере не должны приводить к генетическому загрязнению детерминантами резистентности.
Биохимия резистентности
Существует три основных механизма возникновения антибиотикорезистентности у патогенных для человека бактерий:
– уменьшение внутриклеточного содержания антибиотика в результате снижения проницаемости внешней мембраны, уменьшения транспорта через внутреннюю мембрану или активного эффлюкса;
– индукция ферментативной инактивации препарата;
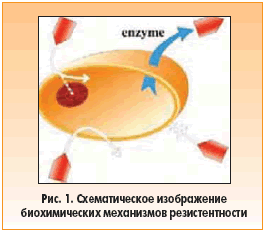
– модифицирование мишени действия антибиотика (рис. 1) [5].
Важно отметить, что ни один их этих механизмов не является специфичным ни для истинной, ни для приобретенной резистентности.
Генетика резистентности
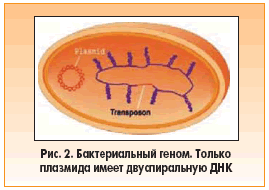
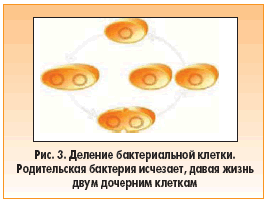
Геном бактериальной клетки состоит из хромосомы, в которой кодируется вся информация, необходимая для жизни бактерии, и дополнительных генетических элементов – плазмид и транспозонов (рис. 2). Последние могут обеспечить организм хозяина генетической информацией (например, детерминантами антибиотикорезистентности), которая ему необходима для выживания в определенных условиях. Чтобы такие генетические элементы были наиболее эффективными на популяционном уровне, они должны передаваться горизонтально между видами или родами. В естественных условиях существует три уровня распространения генов антибиотикорезистентности: бактериальная эпидемия, при которой резистентностью обладает исходный штамм (рис. 3); плазмидная эпидемия, если гены резистентности расположены в конъюгативных плазмидах (рис. 4); генная эпидемия, когда гены являются частью мобильного (подвижного) генетического элемента (рис. 5). В последнем случае, поскольку этот элемент может встраиваться в хромосому хозяина или конъюгативную плазмиду, генетическая информация может наследоваться как вертикально, так и горизонтально. В природе эти три уровня распространения генов резистентности не только не являются взаимоисключающими, но также могут и накладываться друг на друга. Все три механизма резистентности являются экспоненциальными, поскольку включают процесс репликации (дупликации) ДНК, а также способствуют передаче инфекции, поскольку бактерии распространяются среди эукариотов, а мобильные генетические элементы – среди прокариотов.


Потенциальная возможность распространения генов резистентности
Потенциальная возможность распространения генов резистентности значительно варьирует. Она может быть достаточно высокой в том случае, если перенос гена осуществляется мобильным генетическим элементом (например, самопереносимой плазмидой или транспозоном); но может быть и низкой в таких случаях:
· Ген резистентности является хромосомным и отвечает за нечувствительность организма хозяина. Этот ген имеют все представители данного вида или рода, а следовательно, существует возможность проведения точной идентификации бактерии-хозяина.
· Этот ген не может передаваться in vitro или in vivo другим бактериям. Попытки осуществления переноса на модели животных in vivo имеют важное значение, так как, несмотря на существующее мнение, что оптимальные условия создаются в экспериментах по конъюгации in vitro, некоторые гены могут быть успешно перенесены только in vivo [6].
· Отсутствие известных приобретенных генов. Исследования в области антибиотикорезистентности, проведенные за последние 20 лет, вместе с уникальными разработками в области молекулярных технологий позволили выявить и идентифицировать множество различных генов резистентности. Их поиск в интересующих нас пробиотиках может производиться в более (полимеразная цепная реакция со специфическими олигонуклеотидами) или менее строгих (гибридизация или использование вырожденных амплификационных праймеров) условиях.
· Совместная локализация с хромосомной генетической информацией. Потенциальная возможность распространения детерминанты резистентности ниже в том случае, если она стабилизирована в хромосоме. Однако это необходимо продемонстрировать на положительном, а не на отрицательном примере, таком как отсутствие переноса или плазмидная ДНК. Оптимальный способ доказать хромосомную локализацию гена – продемонстрировать его совместную локализацию с генами «домашнего хозяйства» в одном и том же фрагменте ДНК. А наилучшим методом для этого является последовательная гибридизация после расщепления всей ДНК под действием I-Ceu1 (эндонуклеазы рестрикции, которая разрезает гены для рибосомальных РНК) с использованием зондов для интересующих генов и рРНК.
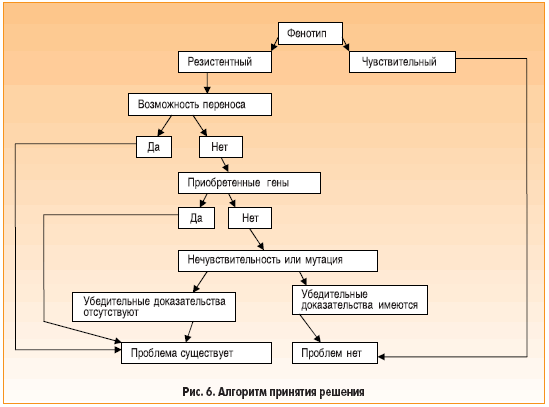
На основании результатов, полученных при использовании различных подходов, можно составить алгоритм принятия решения (рис. 6), который был использован в исследовании по изучению антибиотикорезистентности у Bacillus clausii. Препаратом, содержащим Bacillus, является Enterogermina® [7, 8]. В его состав входят четыре антибиотикорезистентных штамма (OC, NR, T и SIN) [7], которые первоначально были идентифицированы как Bacillus subtilis, однако относительно недавно их отнесли к виду B. clausii [9]. Штаммам Bacillus, входящим в состав препарата Enterogermina®, назначаемого для профилактики кишечных расстройств, была придана полирезистентность к антибиотикам, что позволяет им выжить в условиях одновременного приема антибиотиков [7, 8]. Данные о резистентности четырех штаммов представлены в таблице 1. Наше внимание будет сосредоточено на исследовании резистентности к аминогликозидам (канамицину, тобрамицину и амикацину) у штамма SIN [10].

Оценка риска распространения гена резистентности к аминогликозидам от штамма B. clausii SIN
Оценка проводилась в четыре этапа.
1. Идентификация гена резистентности путем клонирования, определения его нуклеотидной последовательности и сравнительного анализа полученной (аминокислотной) последовательности с имеющимися в базах данных. Геном, отвечающим за резистентность к аминогликозидам, оказался ANT(4′), кодирующий 4′-O-аминогликозидаденилаттрансферазу [ANT(4′)]. Полученный продукт является на 47% тождественным и на 67% сходным с ферментом, полученным из изолята Staphylococcus aureus, а также термофильного штамма Bacillus.
2. Передача гена резистентности. Все попытки передать ген резистентности таким микроорганизмам, как Enterococcus faecalis или Enterococcus faecium, которые являются представителями нормальной кишечной микрофлоры, или B. subtilis, являющегося филогенетически родственным видом, оказались неудачными.
3. Характеристика биохимических механизмов резистентности. Резистентность к аминогликозидам обычно возникает вследствие ферментативной инактивации этих антибиотиков и является широко распространенным явлением среди различных патогенных микроорганизмов. С помощью чувствительных методов эти ферменты могут быть выявлены и охарактеризованы. Один из таких методов анализа подтвердил, что штамм вырабатывает ANT(4′).
4. Определение генетического субстрата резистентности. Предусматривало демонстрацию совместной локализации ANT(4′) с хромосомными генами и подтверждалось данными секвенирования фланкирующей последовательности ДНК, которые указывали на наличие физической связи с хромосомным геном тРНК-синтетазы и отсутствие, по крайней мере, в ближайших к гену участках мобильных генетических элементов, таких как вставочные последовательности, которые могут привести к мобилизации гена.
Результаты исследования представлены в таблице 2 [10, 11]. Были обнаружены различные варианты резистентности:
· Истинная резистентность к пенициллинам, цефалоспоринам, аминогликозидам и макролидам, в основе которой лежат механизмы, характерные и для других видов микроорганизмов, однако кодирующиеся неизвестными генами. Это подтверждает, что B. clausii является бактериальным видом, ранее недостаточно изученным.

· Приобретенная резистентность к тетрациклинам и хлорамфениколу. Генетическая детерминанта для тетрациклина также неизвестна, что указывает на ее недостаточную распространенность среди микроорганизмов, патогенных для человека. Секвенирование пограничных участков детерминанты резистентности к хлорамфениколу свидетельствует о том, что после приобретения она была стабилизирована в хромосоме благодаря перестройке ДНК.
· Резистентность к рифампицину возникает вследствие хромосомной мутации в субъединице β-транскриптазы.
В заключение отметим, что ни один из генов не был связан с известным мобильным генетическим элементом, поэтому риск переноса можно считать минимальным.
Выводы
Вопросы безопасности антимикробной резистентности, которыми долгое время пренебрегали, теперь обязательно учитываются при разработке и маркетинге пробиотиков. В Европе Научный комитет по питанию животных (Scientific Committee on Animal Nutrition, SCAN) в своей резолюции, принятой в 2001 г. и затем пересмотренной в 2002 г., изложил критерии оценки безопасности микроорганизмов, резистентных к антибиотикам, для пробиотиков, используемых у животных [12]. Совсем недавно эти вопросы, которыми занимался Научный комитет, стали компетенцией Европейского агентства по безопасности продуктов питания (European Food Safety Authority, EFSA), которое опубликовало новые рекомендации [13].
Литература
1. Mazza P. The use of Bacillus subtilis as an antidiarrhoeal microorganism. Bull Chim Farm 1994;133: 3-18.
2. Courvalin P., Trieu-Cuot P. Minimizing potential resistance: The molecular view. Clin Infect Dis 2001; 33: S138-46.
3. Courvalin P. Vancomycin resistance in gram-positive cocci. Clin Infect Dis. 2006; 42(Suppl 1): S25-34.
4. Danielsen M., Wind A. Susceptibility of Lactobacillus spp. To antimicrobial agents. Int J Food Microbiol. 2003; 82: 1-11.
5. Guardabassi L., Courvalin P. Antibiotics: Mode of action and mechanisms of resistance. In: Aarestrup F, Wegener HK (editors), Antimicrobial Resistance in Bacteria of Animal Origin. 2006; American Society for Microbiology, Washington DC, pp. 1-18.
6. Launay A., Ballard S.A., Johnson P.D.R., Grayson M.L., Lambert T. Transfer of vancomycin resistance transposon Tn1549 from Clostridium symbiosum to Enterococcus spp. in the gut of gnotobiotic mice. Antimicrob Agents Chemother 2006; 50: 1054-62.
7. Ciffo F. Determination of the spectrum of antibiotic resistance of the «Bacillus subtilis» strains of Enterogermina. Chemioterapia 1984; 3: 45-52.
8. Mazza P., Zani F., Martelli P. Studies on the antibiotic resistance of Bacillus subtilis strains used in oral bacteriotherapy. Bull Chim Farm 1992; 131: 401-8.
9. Senesi S., Celandroni F., Travanti A., Ghelardi E. Molecular characterization and identification of Bacillus clausii strains marketed for use in oral bacteriotherapy. Appl Environ Microbiol 2001; 67: 834-9.
10. Bozdogan B., Galopin S., Gerbaud G., Courvalin P., Leclercq R. Chromosomal aadD2 encodes an aminoglycoside nucleotidyltransferase in Bacillus clausii. Antimicrob Agents Chemother 2003; 47: 1343-6.
11. Bozdogan B., Galopin S., Leclercq R. Characterization of a new erm-related macrolide resistance gene present in probiotic strains of Bacillus clausii. Appl Environ Microbiol. 2004; 70: 280-4.
12. Scientific Committee on Animal Nutrition. Opinion of the Scientific Committee on Animal Nutrition on the criteria for assessing the safety of microorganisms resistant to antibiotics (adopted on 3 July 2001, revised on 24 January 2003). http://ec.europa.eu/comm/food/ fs/sc/scan/out1 08_en.pdf.
13. EFSA. Opinion of the FEEDAP Panel on the updating of the criteria used in the assessment of bacteria for resistance to antibiotics of human or veterinary importance. EFSA J 2005; 223: 1-12. http:// www.efsa.eu.int/science/feedap/feedap_opinions/993_en.html.
Статья впервые напечатана в журнале Digestive and Liver Disease 38 Suppl. 2 (2006) S261-5
health-ua.com









Последние комментарии